Analise o quadro que fornece informações sobre a sacarose, o açúcar de cana.
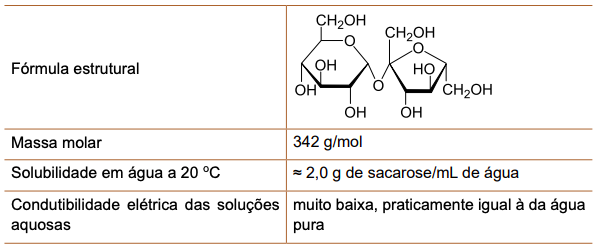
a) Calcule a concentração de uma solução aquosa saturada de sacarose a 20 °C, em g/L de solvente e em mol/kg de solvente.
b) Justifique a alta solubilidade da sacarose em água e a baixa condutibilidade elétrica de suas soluções aquosas.
a) A solubilidade indicada na tabela corresponde à concentração de uma solução aquosa saturada de sacarose a 20oC, que é de 2,0 g de sacarose/mL de água.
Em 1 L (1000 mL) de solvente (água), tem-se:
Para o cálculo da concentração em mol/kg, deve-se calcular a massa molar da sacarose (C12H22O11), que é igual a 342 g/mol.
Como o solvente é a água e a sua densidade 1 kg/L, tem-se que a concentração da solução é de 2000 g de sacarose por 1 kg de solvente.
Assim a concentração em mol/kg é:
b) A alta solubilidade da sacarose em água está associada aos vários grupos hidroxila (-OH) em sua estrutura, sendo uma molécula muito polar e que interage com a água através de ligações de hidrogênio.
A sacarose, um composto molecular, não se ioniza em água, portanto a solução apresenta uma baixa condutibilidade elétrica.