Águas que apresentam alta concentração de íons Ca2+ ou Mg2+ dissolvidos são chamadas de “águas duras”. Se a concentração total desses íons for superior a 100 mg/L, tais águas não podem ser utilizadas em tubulações de máquinas industriais, devido à obstrução dos tubos causada pela formação de sais insolúveis contendo esses íons. Um químico deverá analisar a água de uma fonte, isenta de íons Mg2+, mas contendo íons Ca2+, para verificar se é adequada para uso em uma indústria. Para tal, uma amostra de 200 mL de água dessa fonte foi misturada com uma solução de carbonato de sódio (Na2CO3), em quantidade suficiente para haver reação completa. O sólido formado foi cuidadosamente separado, seco e pesado. A massa obtida foi 0,060 g.
a) Escreva a equação química, na forma iônica, que representa a formação do sólido.
b) A água analisada é adequada para uso industrial? Justifique, mostrando os cálculos.

a) Equação química de formação do sólido
Ca2+(aq) + CO32–(aq) → CaCO3(s)
b) A massa obtida de 0,060 g corresponde ao CaCO3(s) formado. A partir da equação química é possível determinar a massa de Ca2+(aq) existente em 200 mL da solução.
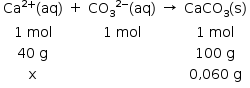
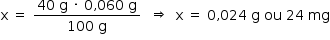
Calculando-se a concentração de Ca2+(aq) na solução
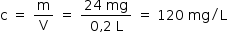
Portanto não pode ser utilizada em tubulações de máquinas industriais.