Um dos pilares da nanotecnologia é o fato de as propriedades dos materiais dependerem do seu tamanho e da sua morfologia. Exemplo: a maior parte do H2 produzido industrialmente advém da reação de reforma de hidrocarbonetos: CH4(g) + H2O(g) → 3H2(g) + CO(g). Uma forma de promover a descontaminação do hidrogênio é reagir o CO com largo excesso de água:
CO(g) + H2O(g) → CO2(g) + H2(g); ΔH = –41,6 kJ mol–1.
A figura abaixo mostra resultados da velocidade (em unidade arbitrária, ua) dessa conversão em função da temperatura, empregando-se um nanocatalisador com duas diferentes morfologias.
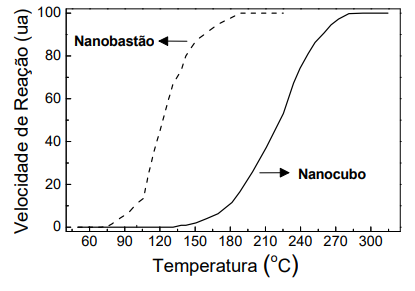
Considerando essas informações, é correto afirmar que, com essa tecnologia, a descontaminação do hidrogênio por CO é mais eficiente na presença do catalisador em forma de
Na descontaminação do H2, o CO deve ser transformado em CO2, de acordo com a equação
De acordo com o gráfico, o nanobastão é mais eficiente, pois a reação apresentará maior velocidade em uma menor temperatura, quando comparada à reação catalisada pelo nanocubo.
Além disso, essa menor temperatura aumentará o rendimento da reação direta no equilíbrio, visto que ela é exotérmica.