Considere a reação entre o íon iodeto e o íon persulfato e a tabela que apresenta dados do estudo de cinética dessa reação.
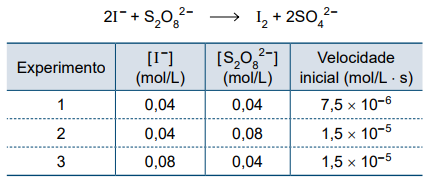
De acordo com os dados obtidos, verifica-se que se trata de uma reação
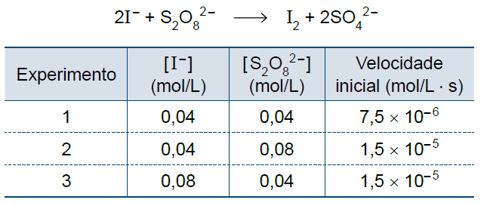
Comparando os experimentos 1 e 2
A concentração de [I-] permanece constante= 0,04 mol/L , e a concentração de dobra ,fazendo com que a velocidade dobre.
Devemos concluir que a ordem da reação em relação à concentração do é igual a 1(reação de 1ª ordem)
Comparando os experimentos 1 e 3
A concentração de permanece constante= 0,04 mol/L , e a concentração de [I-] dobra ,fazendo com que a velocidade dobre.
Devemos concluir que a ordem da reação em relação à concentração do [I-] é igual a 1(reação de 1ª ordem)
Logo podemos concluir que a ordem global da reação é 2 ou 2ªordem, portanto não elementar.