O cinamaldeído é um dos principais compostos que dão o sabor e o aroma da canela. Quando exposto ao ar, oxida conforme a equação balanceada:
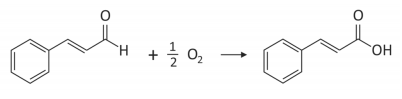
Uma amostra de 19,80 g desse composto puro foi exposta ao ar por 74 dias e depois pesada novamente, sendo que a massa final aumentou em 1,20 g. A porcentagem desse composto que foi oxidada no período foi de
Note e adote:
Massas molares (g/mol):
Cinamaldeído = 132; O2 = 32
Considere que não houve perda de cinamaldeído
ou do produto de oxidação por evaporação.
O aumento de massa de 1,2g está associado à quantidade de O2 que reagiu.
Cálculo da quantidade de cinamaldeído que reagiu:
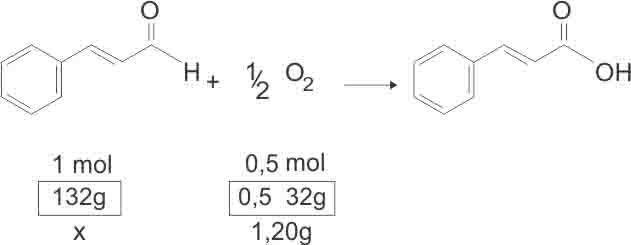
Porcentagem de cinamaldeído que oxidou: