Um resíduo industrial é constituído por uma mistura de carbonato de cálcio (CaCO3) e sulfato de cálcio (CaSO4). O carbonato de cálcio sofre decomposição térmica se aquecido entre 825 e 900 ºC, já o sulfato de cálcio é termicamente estável. A termólise do CaCO3 resulta em óxido de cálcio e gás carbônico.
CaCO3(s) → CaO(s) + CO2(g)
Uma amostra de 10,00 g desse resíduo foi aquecida a 900 ºC até não se observar mais alteração em sua massa. Após o resfriamento da amostra, o sólido resultante apresentava 6,70 g.
O teor de carbonato de cálcio na amostra é de, aproximadamente,
Os 10 gramas de resíduo (mistura de CaSO4 e CaCO3) resultaram numa massa de 6,70 g após o aquecimento, ou seja, houve a perda de 3,3 g de CO2. Com isso é possível determinar a massa de carbonato de cálcio na mistura, visto que apenas ele sofre a decomposição.
CaCO3(s) → CaO(s) + CO2(g)

x = 7,5 de CaCO3 no resíduo.
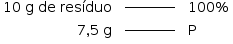
P = 75%