Em laboratório, os peptídeos podem ser sintetizados com reagentes que promovem a ligação entre diferentes aminoácidos. O EDC é um composto que pode ser utilizado em solução aquosa com essa finalidade, como representado a seguir:
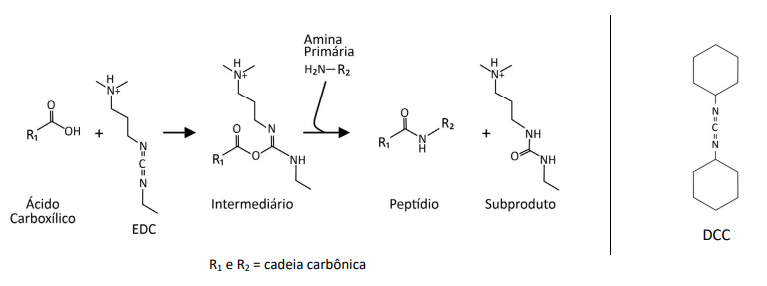
Um reagente similar chamado de DCC, representado acima, também pode ser utilizado para promover o mesmo tipo de reação, mas não é indicado para o uso em meios polares, como soluções aquosas.
a) Escreva, no quadro da folha de respostas, a estrutura do subproduto formado quando DCC é utilizado em substituição ao EDC.
b) O DCC é menos adequado para ser utilizado em solução aquosa do que o EDC por ser menos solúvel. Indique, no quadro da folha de respostas, quais tipos de interações intermoleculares justificam a diferença de solubilidade de cada uma dessas espécies em água.
Um dos métodos utilizados para quantificar proteínas é o método de Kjeldahl, no qual é realizada a determinação da quantidade de matéria nitrogenada total em uma amostra. Esse método consiste em degradar toda a proteína de forma que todos os átomos de nitrogênio da amostra sejam convertidos em sulfato de amônio.
c) Considere uma amostra de 550,2 mg de um peptídeo de fórmula molecular C123H193N35O37 que foi submetida ao método de Kjeldahl. Calcule a quantidade total máxima de mols de sulfato de amônio ((NH4)2SO4) que seria produzida pela análise dessa amostra utilizando esse método.
Note e adote:
Massa molar do C123H193N35O37: 2751 g/mol.
a) Seguindo o modelo de reação apresentado, a estrutura do subproduto, quando se substitui o EDC por DCC, é:
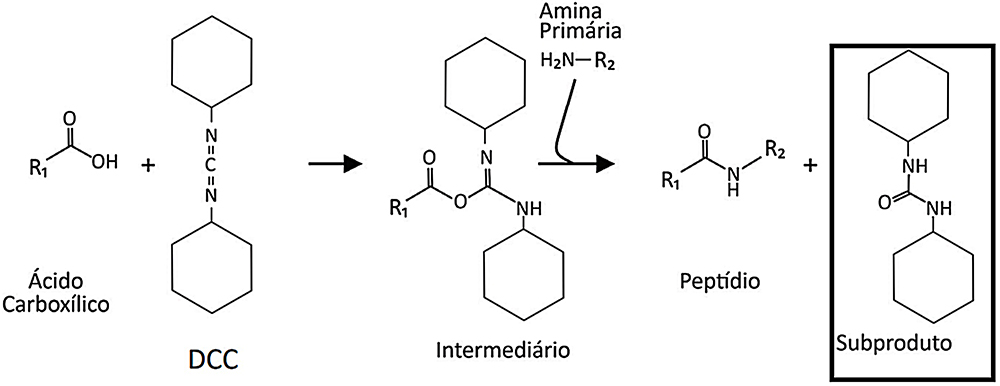
b) O EDC realiza interações do tipo íon-dipolo com água, sendo mais solúvel em água.
O DCC realiza interações do tipo ligações de hidrogênio com a água e também, por possuir uma cadeia carbônica (apolar) maior, apresenta menor solubilidade em água.
c) Segundo o método Kjeldahl, todos os átomos de nitrogênio presentes na proteína são convertidos em sulfato de amônio, conforme a seguinte reação:
Cálculo do número de mol presente em 550,2 mg do peptídeo:
Com base na reação apresentada, a conversão de todos os átomos de nitrogênio presente em 1 mol do peptídeo produz 17,5 mol de sulfato de amônio.
Assim, como na amostra há 2 · 10-4 mol de peptídeo, seguindo a proporção, tem-se 3,5 · 10-3 mol.