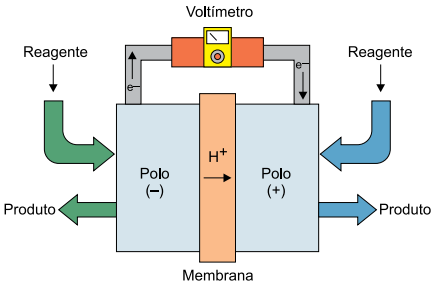
O esquema representa uma célula a combustível de metanol (H3COH). Esse dispositivo eletroquímico funciona como uma pilha com alimentação contínua dos reagentes nos compartimentos anódico e catódico, os quais são separados por uma membrana condutora de íons que tem a função da ponte salina.
As semirreações dos reagentes que são inseridos nessa célula a combustível estão representadas no sentido da redução, com os respectivos potenciais padrão de redução, Eo:
O2 (g) + 2H+ (aq) + 2 e– → H2O (ℓ) Eo = + 1,229 V
CO2 (g) + 6H+ (aq) + 6 e– → H3COH (ℓ) + H2O (ℓ) Eo = + 0,046 V
a) Calcule os números de oxidação dos átomos de carbono do metanol e do dióxido de carbono.
b) Apresente a equação global dessa célula a combustível. Calcule a diferença de potencial padrão dessa célula.
a) Os números de oxidação do carbono são:
b) Semiequação de redução:
Semiequação de oxidação:
Equação global:
A diferença de potencial padrão da célula é: