Para esfriar um copo contendo 250 mL de água fervente (100°C), é comum utilizar o seguinte método:
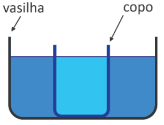
Passo 1. Colocar esse copo dentro de uma vasilha em contato com 1 litro de água à temperatura ambiente (25°C), como mostrado na figura.
Passo 2. Esperar que entrem em equilíbrio térmico.
Passo 3. Tirar o copo e trocar a água da vasilha por outro litro de água à temperatura ambiente.
Passo 4. Colocar o copo em contato com a água “nova” e esperar que entrem em equilíbrio térmico.
Após o passo (4) desse método, a temperatura da água no copo será aproximadamente:
Note e adote:
Considere apenas trocas de calor entre a água no copo e a água na vasilha. Despreze quaisquer trocas de calor do sistema com o ambiente.
Durante os passos 1 e 2, a água no copo libera calor (Q1) e diminui a sua temperatura de 100 ºC até uma temperatura de equilíbrio (θeq). Simultaneamente, a água na vasilha recebe calor (Q2) e aumenta sua temperatura de 25 ºC até atingir a mesma temperatura (θeq), conforme ilustrado na figura a seguir.

De acordo com o “note e adote” da questão, há trocas de calor apenas entre a água no copo e a água na vasilha. Nesse contexto, o sistema é termicamente isolado, assim:
Durante os passos 3 e 4, a água no copo libera calor (Q1´) e diminui a sua temperatura de 40 ºC até uma temperatura de equilíbrio (θeq´). Simultaneamente, a água na vasilha recebe calor (Q2´) e aumenta sua temperatura de 25 ºC até atingir a mesma temperatura (θeq´), conforme ilustrado na figura a seguir.

Como o sistema é termicamente isolado, então: