Para gerar hidrogênio, foi utilizado o aparato ilustrado na figura.
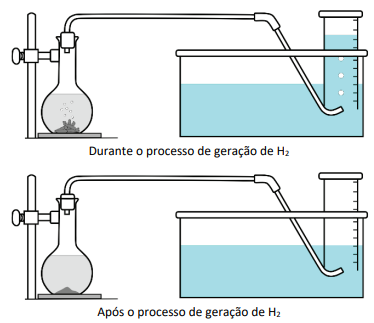
Ao frasco à esquerda adicionou-se uma quantidade prédeterminada de raspas de zinco metálico e ácido clorídrico. Em seguida, o frasco foi fechado com uma rolha conectada a uma tubulação. À medida que o hidrogênio é produzido pela reação Zn0(s) + 2H+(aq) → Zn2+(aq) + H2(g), o gás se acumula em uma proveta previamente cheia de água. Dado que a solubilidade do hidrogênio na água é desprezível, o volume ocupado pelo gás na proveta corresponde ao volume de hidrogênio produzido durante a reação.
Considerando que, nas condições do experimento, foram gerados 49,8 mL de hidrogênio, qual a quantidade de Zn metálico, em gramas, que de fato reagiu?
Para calcular a quantidade de zinco metálico, em gramas, que reagiu para produzir 49,8 mL de hidrogênio, pode-se usar a equação balanceada da reação: